3'50" 읽기
- 1990년대 개발된 1세대 CAR-T 세포는 미미한 효과만 있는 것으로 입증
- 현재까지 5개의 CAR-T 세포 치료제가 미국과 EU에서 승인
- 초기 성공에도 불구하고 CAR-T 치료법은 지금까지 혈액이나 림프에 자유롭게 떠다니는 암세포에만 효과적
맞춤형 도킹 포인트
1990년대에 개발된 이 CAR-T-세포 요법은 암 환자의 T 세포에 소위 키메라 항원 수용체(CAR)를 제공하는 유전 공학 프로세스를 기반으로 한다. 이들은 주로 T 세포의 활성화 수용체에 부착된 암 특이적 항체의 두 사슬로 구성된다. 방어 세포가 이 결합된 수용체와 함께 암세포에 도킹하면 T 세포에서 신호 캐스케이드가 트리거되어 T 세포를 활성화하고 세포 독성 메커니즘을 작동시킨다.
그러나 실제로는 이러한 1세대 CAR-T 세포는 미미한 효과만 있는 것으로 입증됐다. 이러한 방식으로 조작된 T 세포는 충분히 증식하지 못하고 너무 비활성 상태로 남아 있었다. 이러한 이유로 이후 인공 도킹 사이트가 T 세포 내부의 추가 자극 신호 모듈에 연결된 2세대 및 3세대 CAR 변이체가 개발됐다.
순서
암 환자의 T 세포에 이러한 키메라 수용체를 장착하기 위해 환자로부터 혈액을 채취하고 T 세포를 분리한다. 바이러스 유전자 셔틀은 추가 수용체에 필요한 유전자를 이러한 T 세포의 게놈에 삽입하기 위해 실험실에서 사용된다. 이런 방식으로 유전적으로 변형된 T 세포는 이제 원하는 표면과 신호 분자 자체를 생산한다. 이들은 CAR-T-세포가 된다.
CAR-T 세포는 이제 실험실에서 증식된 다음 주입을 통해 환자에게 다시 제공된다. 이러한 "업그레이드된" T 세포가 체내에서 자기주장을 할 수 있으려면 암 환자가 먼저 화학 요법을 받아야 한다. 이것은 일부 암세포와 암에 적응하지 못한 신체 자체의 T 세포를 제거한다. 따라서 CAR-T 세포가 체내에서 충분히 증식될 때까지 환자는 약 2주 동안 면역이 심하게 저하된다. 그 후 치료가 점차 효과를 발휘하고 "업그레이드된" T 세포가 암세포를 공격하고 파괴하기 시작한다.
백혈병 및 림프종에 대해 승인됨
현재까지 5개의 CAR-T 세포 치료제가 미국과 EU에서 승인되었다. 이들은 환자의 B 세포가 퇴화되어 현재의 암 요법에 반응하지 않는 림프종 및 백혈병을 치료하는 데 사용된다. 현재까지 가장 일반적으로 사용되는 CAR-T 치료법인 tisagenlecleucel(Kymriah)은 임상 시험에서 치료받은 백혈병 환자의 80%에서 관해를 달성했다. B 세포 림프종에 사용되는 Axicabtagene ciloleucel(Yescarta) 요법은 환자의 65%에서 최소 1년의 무재발률을 보였다.
그러나 CAR-T 세포 치료제에 부작용이 없는 것은 아니다. CAR-T 세포의 활성화 및 증식은 일반적으로 전염증성 사이토카인의 강력한 방출로 이어진다. 바이러스 감염에 의해 유발되는 사이토카인 폭풍과 유사하게 이 사이토카인 방출 증후군은 독감 유사 증상에서 심각한 전신 염증에 이르는 증상을 유발할 수 있다. 또한 관문 억제제와 마찬가지로 T세포의 강력한 활성화는 면역계의 과민반응을 유발할 수 있다.
고형 종양에 대한 기갑 CAR-T 세포
초기 성공에도 불구하고 CAR-T 치료법은 지금까지 혈액이나 림프에 자유롭게 떠다니는 암세포에만 효과적이었다. 반면에 고형 종양에 대해서는 효과가 제한적이거나 전혀 없다. "고형 종양에서 T 세포는 암 초점에 도달하기 위해 몇 가지 장벽을 극복해야 한다"고 런던 암 연구소의 Elizabeth Hawkings는 설명한다. 결과적으로 방어 세포는 종종 치밀한 종양 조직에 침투하는 데 어려움을 겪는다. "그러나 T 세포가 이것을 하는 데 성공하더라도, 그들은 면역억제성이 높은 종양 미세 환경에 직면하게 된다"고 Hawkings는 말했다. 암세포는 T 세포를 고정시키고 무력화시키는 메신저 물질을 방출한다.
이를 방지하기 위해 과학자들은 이미 새로운 4세대 CAR 요법을 연구하고 있다. 이 경우 T 세포는 추가 "무기"를 갖추고 있다. 암세포와 접촉하면 키메라 항원 수용체도 면역 활성화 메신저 물질과 때로는 체크포인트 억제제의 방출을 활성화한다. 결과적으로 T 세포는 자체적으로 항체를 생성하여 "브레이크"를 해제하고 활동을 상향 조절한다. 이러한 무장한 CAR-T 세포를 사용한 첫 번째 치료법이 테스트되고 있지만 아직 승인되지 않았다.
노력의 문제
그러나 또 다른 문제가 있다. CAR-T 세포 요법은 너무 복잡하고 비싸서 아직 널리 사용되지 않았다. 이것은 주로 T 세포의 개인별, 환자별 생산 때문이다. 예를 들어, B세포 백혈병 치료에 사용되는 티사젠렉류셀 요법은 독일에서 간접 비용을 포함하지 않고 환자당 45만 유로 이상의 비용이 들 수 있다. 다른 CAR 치료법은 거의 저렴하지 않다. 또한 소수의 의료 센터에서만 이 치료법을 제공할 수 있다. 현재 독일의 약 15개 대학 클리닉만이 필요한 기술과 인증을 보유하고 있다.
시간적 요인도 있다. 암 환자의 T 세포를 전환하는 데 약 3주가 걸린다. CAR-T 치료를 전문으로 하는 텍사스 대학의 암 연구원 Sattva Neelapu는 최근 이러한 치료를 받는 환자의 약 10~15%가 T 세포를 사용할 수 있을 때 사망하거나 너무 아프다고 추정했다.
바이러스 유전자 셔틀 대신 유전자 가위
이 문제를 극복하기 위해 연구자들은 현재 T 세포의 유전 공학을 위한 새롭고 빠르고 저렴한 방법을 연구하고 있다. 예를 들어, 2022년에 로스앤젤레스 캘리포니아 대학의 Antoni Ribas가 이끄는 팀은 바이러스 유전자 셔틀이 아닌 CRISPR/Cas9 유전자 가위로 16명의 환자의 T 세포를 유전자 변형했다.
이점:
이 절차를 통해 새로운 CAR 모듈의 유전자를 방어 세포의 게놈에 통합할 수 있고 세포 자체의 덜 효과적인 수용체 유전자를 한 번에 절제할 수 있다. 그러나 고형 종양에 대해 이 방법을 사용하려는 시도는 부분적으로만 효과적이었다. 암은 16명의 환자 중 11명에서 계속 성장했다. 그러나 Ribas와 그의 팀은 추가 최적화를 위해 노력하고 있으며 효율성을 높일 수 있다고 확신한다.
자신의 T 세포가 아닌 외부 T 세포?
또 다른 접근법은 환자의 개별 T 세포를 사용하지 않고 이전에 실험실에서 증식시킨 건강한 기증자의 T 세포를 대신 사용하여 CAR 요법을 더 표준화하는 것이다. 이것은 이 치료법이 더 저렴하고 간단하며 암이나 화학 요법으로 이미 T 세포가 너무 많이 손상된 암 환자에게도 사용될 수 있다는 이점이 있다. 그러나 단점은 면역 체계가 외부 T 세포를 공격하므로 이식과 유사하게 면역 억제제로 억제해야 한다는 것입니다. 그러나 이것은 환자를 감염에 취약하게 만들고 종양에도 도움이 될 수 있다.
2020년에 그러한 동종이계 CAR-T 세포를 사용한 첫 번째 1상 연구가 유망한 결과를 낳았다. 22명의 림프종 환자에서 종양이 줄어들었고 환자의 40%에서 종양이 완전히 사라졌다. Neelapu는 "Nature"에 "반응률은 신체 자체 세포를 사용한 CAR-T 요법과 거의 동일했다"고 보고했다. 부작용도 비슷했다. 그러나 이 치료법은 아직 초기 단계다. 그러한 표준화된 CAR T-세포 치료법이 언젠가 암에 대항하는 중요한 무기가 될지는 두고 볼 일이다. (계속)
- 1990년대 개발된 1세대 CAR-T 세포는 미미한 효과만 있는 것으로 입증
- 현재까지 5개의 CAR-T 세포 치료제가 미국과 EU에서 승인
- 초기 성공에도 불구하고 CAR-T 치료법은 지금까지 혈액이나 림프에 자유롭게 떠다니는 암세포에만 효과적
업그레이드된 방어 세포: CAR-T 세포치료제 원리
면역 체계의 T 세포는 또한 암에 대한 면역 요법의 또 다른 변이체 역할을 한다. 많은 종양이 위장되어 있기 때문에 스스로 인식하고 공격하지 않으므로 인위적으로 "무장"된다. 암세포에 도킹하여 죽이는 데 필요한 수용체를 유전적으로 갖추고 있다.
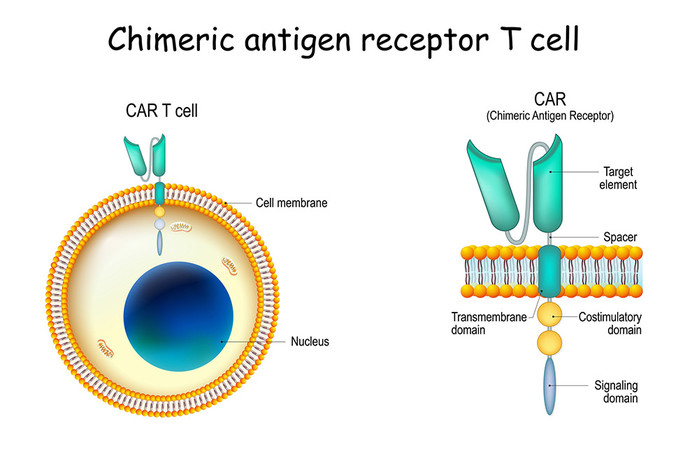 |
| ▲ CAR-T 세포 요법은 암 환자의 T 세포에 종양 특이적 항원 도킹 사이트를 장착한다. 이를 통해 암세포를 더 잘 탐지하고 싸울 수 있다. © ttsz/ 게티 이미지 |
맞춤형 도킹 포인트
1990년대에 개발된 이 CAR-T-세포 요법은 암 환자의 T 세포에 소위 키메라 항원 수용체(CAR)를 제공하는 유전 공학 프로세스를 기반으로 한다. 이들은 주로 T 세포의 활성화 수용체에 부착된 암 특이적 항체의 두 사슬로 구성된다. 방어 세포가 이 결합된 수용체와 함께 암세포에 도킹하면 T 세포에서 신호 캐스케이드가 트리거되어 T 세포를 활성화하고 세포 독성 메커니즘을 작동시킨다.
그러나 실제로는 이러한 1세대 CAR-T 세포는 미미한 효과만 있는 것으로 입증됐다. 이러한 방식으로 조작된 T 세포는 충분히 증식하지 못하고 너무 비활성 상태로 남아 있었다. 이러한 이유로 이후 인공 도킹 사이트가 T 세포 내부의 추가 자극 신호 모듈에 연결된 2세대 및 3세대 CAR 변이체가 개발됐다.
순서
암 환자의 T 세포에 이러한 키메라 수용체를 장착하기 위해 환자로부터 혈액을 채취하고 T 세포를 분리한다. 바이러스 유전자 셔틀은 추가 수용체에 필요한 유전자를 이러한 T 세포의 게놈에 삽입하기 위해 실험실에서 사용된다. 이런 방식으로 유전적으로 변형된 T 세포는 이제 원하는 표면과 신호 분자 자체를 생산한다. 이들은 CAR-T-세포가 된다.
CAR-T 세포는 이제 실험실에서 증식된 다음 주입을 통해 환자에게 다시 제공된다. 이러한 "업그레이드된" T 세포가 체내에서 자기주장을 할 수 있으려면 암 환자가 먼저 화학 요법을 받아야 한다. 이것은 일부 암세포와 암에 적응하지 못한 신체 자체의 T 세포를 제거한다. 따라서 CAR-T 세포가 체내에서 충분히 증식될 때까지 환자는 약 2주 동안 면역이 심하게 저하된다. 그 후 치료가 점차 효과를 발휘하고 "업그레이드된" T 세포가 암세포를 공격하고 파괴하기 시작한다.
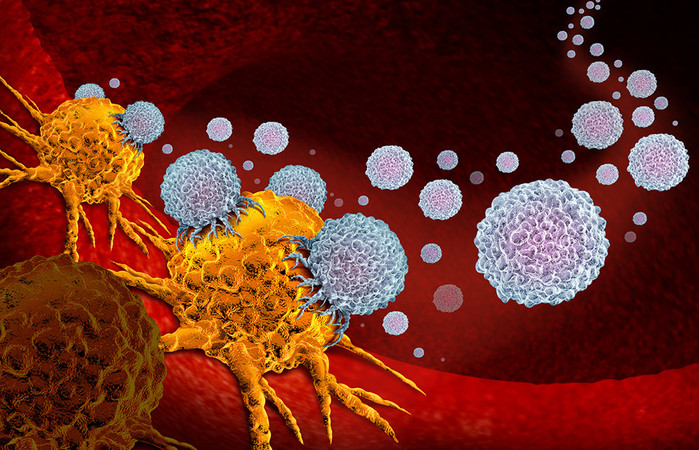 |
| ▲ CAR 수용체가 장착된 Z 세포는 암세포를 특이적으로 공격한다. © wildpixel/ 게티 이미지 |
백혈병 및 림프종에 대해 승인됨
현재까지 5개의 CAR-T 세포 치료제가 미국과 EU에서 승인되었다. 이들은 환자의 B 세포가 퇴화되어 현재의 암 요법에 반응하지 않는 림프종 및 백혈병을 치료하는 데 사용된다. 현재까지 가장 일반적으로 사용되는 CAR-T 치료법인 tisagenlecleucel(Kymriah)은 임상 시험에서 치료받은 백혈병 환자의 80%에서 관해를 달성했다. B 세포 림프종에 사용되는 Axicabtagene ciloleucel(Yescarta) 요법은 환자의 65%에서 최소 1년의 무재발률을 보였다.
그러나 CAR-T 세포 치료제에 부작용이 없는 것은 아니다. CAR-T 세포의 활성화 및 증식은 일반적으로 전염증성 사이토카인의 강력한 방출로 이어진다. 바이러스 감염에 의해 유발되는 사이토카인 폭풍과 유사하게 이 사이토카인 방출 증후군은 독감 유사 증상에서 심각한 전신 염증에 이르는 증상을 유발할 수 있다. 또한 관문 억제제와 마찬가지로 T세포의 강력한 활성화는 면역계의 과민반응을 유발할 수 있다.
고형 종양에 대한 기갑 CAR-T 세포
초기 성공에도 불구하고 CAR-T 치료법은 지금까지 혈액이나 림프에 자유롭게 떠다니는 암세포에만 효과적이었다. 반면에 고형 종양에 대해서는 효과가 제한적이거나 전혀 없다. "고형 종양에서 T 세포는 암 초점에 도달하기 위해 몇 가지 장벽을 극복해야 한다"고 런던 암 연구소의 Elizabeth Hawkings는 설명한다. 결과적으로 방어 세포는 종종 치밀한 종양 조직에 침투하는 데 어려움을 겪는다. "그러나 T 세포가 이것을 하는 데 성공하더라도, 그들은 면역억제성이 높은 종양 미세 환경에 직면하게 된다"고 Hawkings는 말했다. 암세포는 T 세포를 고정시키고 무력화시키는 메신저 물질을 방출한다.
이를 방지하기 위해 과학자들은 이미 새로운 4세대 CAR 요법을 연구하고 있다. 이 경우 T 세포는 추가 "무기"를 갖추고 있다. 암세포와 접촉하면 키메라 항원 수용체도 면역 활성화 메신저 물질과 때로는 체크포인트 억제제의 방출을 활성화한다. 결과적으로 T 세포는 자체적으로 항체를 생성하여 "브레이크"를 해제하고 활동을 상향 조절한다. 이러한 무장한 CAR-T 세포를 사용한 첫 번째 치료법이 테스트되고 있지만 아직 승인되지 않았다.
노력의 문제
그러나 또 다른 문제가 있다. CAR-T 세포 요법은 너무 복잡하고 비싸서 아직 널리 사용되지 않았다. 이것은 주로 T 세포의 개인별, 환자별 생산 때문이다. 예를 들어, B세포 백혈병 치료에 사용되는 티사젠렉류셀 요법은 독일에서 간접 비용을 포함하지 않고 환자당 45만 유로 이상의 비용이 들 수 있다. 다른 CAR 치료법은 거의 저렴하지 않다. 또한 소수의 의료 센터에서만 이 치료법을 제공할 수 있다. 현재 독일의 약 15개 대학 클리닉만이 필요한 기술과 인증을 보유하고 있다.
시간적 요인도 있다. 암 환자의 T 세포를 전환하는 데 약 3주가 걸린다. CAR-T 치료를 전문으로 하는 텍사스 대학의 암 연구원 Sattva Neelapu는 최근 이러한 치료를 받는 환자의 약 10~15%가 T 세포를 사용할 수 있을 때 사망하거나 너무 아프다고 추정했다.
바이러스 유전자 셔틀 대신 유전자 가위
이 문제를 극복하기 위해 연구자들은 현재 T 세포의 유전 공학을 위한 새롭고 빠르고 저렴한 방법을 연구하고 있다. 예를 들어, 2022년에 로스앤젤레스 캘리포니아 대학의 Antoni Ribas가 이끄는 팀은 바이러스 유전자 셔틀이 아닌 CRISPR/Cas9 유전자 가위로 16명의 환자의 T 세포를 유전자 변형했다.
이점:
이 절차를 통해 새로운 CAR 모듈의 유전자를 방어 세포의 게놈에 통합할 수 있고 세포 자체의 덜 효과적인 수용체 유전자를 한 번에 절제할 수 있다. 그러나 고형 종양에 대해 이 방법을 사용하려는 시도는 부분적으로만 효과적이었다. 암은 16명의 환자 중 11명에서 계속 성장했다. 그러나 Ribas와 그의 팀은 추가 최적화를 위해 노력하고 있으며 효율성을 높일 수 있다고 확신한다.
자신의 T 세포가 아닌 외부 T 세포?
또 다른 접근법은 환자의 개별 T 세포를 사용하지 않고 이전에 실험실에서 증식시킨 건강한 기증자의 T 세포를 대신 사용하여 CAR 요법을 더 표준화하는 것이다. 이것은 이 치료법이 더 저렴하고 간단하며 암이나 화학 요법으로 이미 T 세포가 너무 많이 손상된 암 환자에게도 사용될 수 있다는 이점이 있다. 그러나 단점은 면역 체계가 외부 T 세포를 공격하므로 이식과 유사하게 면역 억제제로 억제해야 한다는 것입니다. 그러나 이것은 환자를 감염에 취약하게 만들고 종양에도 도움이 될 수 있다.
2020년에 그러한 동종이계 CAR-T 세포를 사용한 첫 번째 1상 연구가 유망한 결과를 낳았다. 22명의 림프종 환자에서 종양이 줄어들었고 환자의 40%에서 종양이 완전히 사라졌다. Neelapu는 "Nature"에 "반응률은 신체 자체 세포를 사용한 CAR-T 요법과 거의 동일했다"고 보고했다. 부작용도 비슷했다. 그러나 이 치료법은 아직 초기 단계다. 그러한 표준화된 CAR T-세포 치료법이 언젠가 암에 대항하는 중요한 무기가 될지는 두고 볼 일이다. (계속)
[더사이언스플러스=문광주 기자]
[저작권자ⓒ the SCIENCE plus. 무단전재-재배포 금지]
주요기사
+
많이 본 기사
Basic Science
+
AI & Tech
+
Photos
+