3'320"읽기
- 연구원들, 바이러스 스파이크 단백질의 403번 위치에 있는 아미노산을 자세히 조사
- 아미노산의 표적 돌연변이(위치 403)는 박쥐 코로나바이러스가 SARS-CoV-2와 동일한 수용체인 인간 ACE2 수용체에 도킹할 수 있게 한다.
- mRNA백신은 돌연변이 박쥐 바이러스에 효과 있을 것이다.
전염병 병원체 SARS-CoV-2는 어떤 동물 코로나바이러스에서 발생했을까?
현재까지 이에 대한 명확한 답은 없다. 중국 윈난성의 편자코에서 분리되고 우한의 바이러스 연구소에서 배양된 균주 RaTG13은 SARS-CoV-2와 유전적으로 96% 일치한다. 그러나 인간 세포의 ACE2 수용체와 도킹할 수 없다.
이것은 천산갑에서 분리된 2개의 코로나바이러스와 라오스의 박쥐에서 분리된 3개의 바이러스 변종과 다르다. 후자는 인간 세포에 결합할 뿐만 아니라 RaTG13보다 SARS-CoV-2, 특히 바이러스 스파이크 단백질의 수용체 결합 도메인에 더 유사하다. 따라서 라오스에서 온 세 가지 BAAL로 불리는 코로나바이러스는 현재 대유행 병원체의 가장 가까운 친척으로 여겨진다.
관찰 403번 위치
그러나 세 가지 라오스 바이러스인 RaTG13과 SARS-CoV-2의 결정적인 차이점은 어디에 있을까? 더 자세히 알아보기 위해 울름 대학의 Fabian Zech와 그의 동료들은 바이러스 스파이크 단백질의 403번 위치에 있는 아미노산을 자세히 조사했다.
연구진은 "이전 시뮬레이션에서는 R403이 SARS-CoV-2 결합 도메인과 ACE2 수용체의 상호작용에 크게 기여한다고 제안했다"고 설명했다.
유행성 병원체 SARS-CoV-2와 그 전신인 SARS-CoV는 모두 403번 위치에 양전하를 띤 아미노산인 아르기닌(R) 또는 라이신(K)을 가지고 있다. 이 단백질 구성요소의 모양과 양전하로 인해 인간 ACE2 수용체의 글루탐산 빌딩 블록과 밀접하게 상호작용할 수 있다. 반면에 RaTG13은 다르다. 403번 위치에 아미노산 트레오닌(T)이 있고 중성 측쇄가 있다.
교환된 아미노산
그러나 박쥐 바이러스 RaTG13에서 아미노산 트레오닌을 아르기닌으로 바꾸면 어떻게 될까요? 이를 테스트하기 위해 팀은 RaTG13의 스파이크 단백질과 이러한 T403R 돌연변이로 슈도바이러스를 만들었다. 비교를 위해 역 돌연변이를 가진 SARS-CoV-2 슈도바이러스를 생산했다. 그런 다음 두 가지 유형의 바이러스를 인간 세포 배양에 추가했다.
놀라운 결과:
RaTG13은 일반적으로 인간 세포에 결합할 수 없지만 T403R 돌연변이가 있는 박쥐 슈도바이러스의 경우였다. 선임 저자인 Frank Kirchhoff는 "RaTG13의 스파이크 단백질에 있는 아미노산의 표적 돌연변이(더 정확하게는 위치 403)는 이 박쥐 코로나바이러스가 SARS-CoV-2와 동일한 수용체인 인간 ACE2 수용체에 도킹할 수 있도록 한다"고 말했다.
감염성을 위한 결정적인 빌딩 블록
이전에 생각했던 것과는 대조적으로, 이 하나의 돌연변이는 RaTG13이 인간 세포를 감염시키기에 충분하다. SARS-CoV-2와 유사하게 돌연변이 박쥐 바이러스도 감염된 세포의 융합을 촉발했다. "RaTG13에서 T403R 교환의 강력한 효과는 놀랍게도 SARS-CoV-2의 ACE2 수용체 결합에 결정적인 것으로 간주된 6개의 단백질 구성 요소 중 5개가 RaTG13에 존재하지 않기 때문이다"고 팀은 보고했다.
이것은 위치 403의 양전하를 띤 아미노산이 평균 이상으로 중요함을 시사한다. 이것은 역 교환에 의해 확인됐다. Zech와 그의 동료들이 발견한 바와 같이 아르기닌 대신 트레오닌이 포함된 SARS-CoV-2 슈도바이러스는 감염성이 감소했다. 대유행 병원체는 그렇지 않으면 우리 세포에 최적으로 적응되지만, 이 하나의 돌연변이는 결합 능력을 감소시키기에 충분했다.
추가 종 점프에 대한 요구 사항?
연구팀은 코로나바이러스의 종 도약을 위한 결정적인 단계를 찾을 수 있었다.
Zech와 그의 동료들은 "종합적으로 볼 때, 우리의 결과는 스파이크 단백질의 위치 403에 있는 양성 아미노산 단위가 효율적인 인수공통전염병 전염과 SARS-CoV-2의 대유행 확산을 위한 전제 조건임을 시사한다"고 기술했다.
동시에 이 결과는 동물계와 특히 박쥐에 이미 이 중요한 특성을 가진 많은 코로나바이러스가 있을 수 있음을 시사한다. 라오스 박쥐 바이러스와 천산갑 바이러스도 자연적으로 403번 위치에 양전하를 띤 아미노산을 가지고 있다.
최소한의 위안: 보충 테스트에서 백신 접종 및 회복기 환자의 인간 혈청 항체도 RaTG13의 인위적으로 돌연변이된 균주에 대해 작용했다. 많은 유전적 차이에도 불구하고 현재의 코로나 백신은 밀접하게 관련된 코로나바이러스와 미래의 인수공통전염병으로부터 보호할 수도 있다.
"따라서 Covid-19 백신 접종은 그러한 바이러스 병원체가 미래에 인간에게 퍼지는 것을 방지하는 데 도움이 될 수 있다"고 Zech와 그의 동료들이 설명했다.
(Nature Communications, 2021; doi: 10.1038 / s41467-021-27180-0)
출처: Universität Ulm
- 연구원들, 바이러스 스파이크 단백질의 403번 위치에 있는 아미노산을 자세히 조사
- 아미노산의 표적 돌연변이(위치 403)는 박쥐 코로나바이러스가 SARS-CoV-2와 동일한 수용체인 인간 ACE2 수용체에 도킹할 수 있게 한다.
- mRNA백신은 돌연변이 박쥐 바이러스에 효과 있을 것이다.
코로나바이러스: 하나의 아미노산으로 충분하다.
스파이크 단백질의 구성 요소를 교체하면 박쥐 바이러스 RaTG13이 우리에게 전염된다.
놀랍게도 간단하다.
박쥐 코로나바이러스에서 SARS-CoV-2와 같은 인간 병원성 형태로의 단계는 예상보다 작을 수 있다. 바이러스 스파이크 단백질의 중요한 아미노산을 교체하면 RaTG13 박쥐 바이러스가 인간 세포를 감염시킬 수 있다. 적어도 안심할 수 있는 것은 연구원들이 발견한 바와 같이 우리의 mRNA 백신이 이 돌연변이 박쥐 바이러스에 대해서도 효과적일 것이라는 점이다.
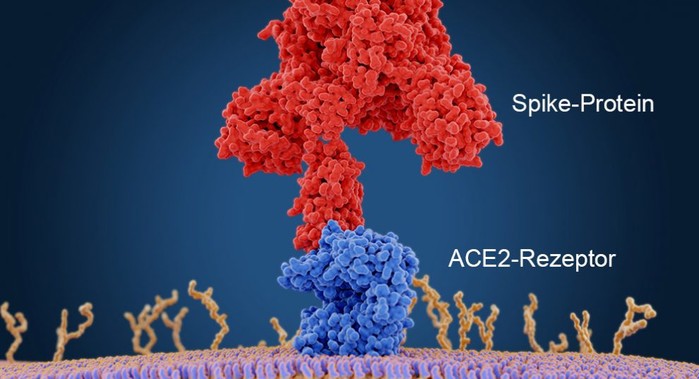 |
▲ 코로나바이러스가 우리 세포에 도킹하려면 바이러스 스파이크 단백질의 결합 도메인이 ACE2 수용체와 일치해야 한다. © selvanegra / 게티 이미지 |
전염병 병원체 SARS-CoV-2는 어떤 동물 코로나바이러스에서 발생했을까?
현재까지 이에 대한 명확한 답은 없다. 중국 윈난성의 편자코에서 분리되고 우한의 바이러스 연구소에서 배양된 균주 RaTG13은 SARS-CoV-2와 유전적으로 96% 일치한다. 그러나 인간 세포의 ACE2 수용체와 도킹할 수 없다.
이것은 천산갑에서 분리된 2개의 코로나바이러스와 라오스의 박쥐에서 분리된 3개의 바이러스 변종과 다르다. 후자는 인간 세포에 결합할 뿐만 아니라 RaTG13보다 SARS-CoV-2, 특히 바이러스 스파이크 단백질의 수용체 결합 도메인에 더 유사하다. 따라서 라오스에서 온 세 가지 BAAL로 불리는 코로나바이러스는 현재 대유행 병원체의 가장 가까운 친척으로 여겨진다.
관찰 403번 위치
그러나 세 가지 라오스 바이러스인 RaTG13과 SARS-CoV-2의 결정적인 차이점은 어디에 있을까? 더 자세히 알아보기 위해 울름 대학의 Fabian Zech와 그의 동료들은 바이러스 스파이크 단백질의 403번 위치에 있는 아미노산을 자세히 조사했다.
연구진은 "이전 시뮬레이션에서는 R403이 SARS-CoV-2 결합 도메인과 ACE2 수용체의 상호작용에 크게 기여한다고 제안했다"고 설명했다.
유행성 병원체 SARS-CoV-2와 그 전신인 SARS-CoV는 모두 403번 위치에 양전하를 띤 아미노산인 아르기닌(R) 또는 라이신(K)을 가지고 있다. 이 단백질 구성요소의 모양과 양전하로 인해 인간 ACE2 수용체의 글루탐산 빌딩 블록과 밀접하게 상호작용할 수 있다. 반면에 RaTG13은 다르다. 403번 위치에 아미노산 트레오닌(T)이 있고 중성 측쇄가 있다.
 |
| ▲ ACE2 수용체 상의 글루탐산(E37)과 SARS-CoV-2 및 RaTG13의 스파이크 단백질 상의 아미노산 아르기닌(R403) 또는 트레오닌(T403) 간의 상호작용. © Zech et al./ Nature Communications, CC-by-sa 4.0 (출처: 관련논문 Fig. 1: Modelling of the interaction of Coronavirus Spike residue 403 with human ACE2. / Spike residue 403 affects binding of coronavirus spikes to human ACE2) |
교환된 아미노산
그러나 박쥐 바이러스 RaTG13에서 아미노산 트레오닌을 아르기닌으로 바꾸면 어떻게 될까요? 이를 테스트하기 위해 팀은 RaTG13의 스파이크 단백질과 이러한 T403R 돌연변이로 슈도바이러스를 만들었다. 비교를 위해 역 돌연변이를 가진 SARS-CoV-2 슈도바이러스를 생산했다. 그런 다음 두 가지 유형의 바이러스를 인간 세포 배양에 추가했다.
놀라운 결과:
RaTG13은 일반적으로 인간 세포에 결합할 수 없지만 T403R 돌연변이가 있는 박쥐 슈도바이러스의 경우였다. 선임 저자인 Frank Kirchhoff는 "RaTG13의 스파이크 단백질에 있는 아미노산의 표적 돌연변이(더 정확하게는 위치 403)는 이 박쥐 코로나바이러스가 SARS-CoV-2와 동일한 수용체인 인간 ACE2 수용체에 도킹할 수 있도록 한다"고 말했다.
감염성을 위한 결정적인 빌딩 블록
이전에 생각했던 것과는 대조적으로, 이 하나의 돌연변이는 RaTG13이 인간 세포를 감염시키기에 충분하다. SARS-CoV-2와 유사하게 돌연변이 박쥐 바이러스도 감염된 세포의 융합을 촉발했다. "RaTG13에서 T403R 교환의 강력한 효과는 놀랍게도 SARS-CoV-2의 ACE2 수용체 결합에 결정적인 것으로 간주된 6개의 단백질 구성 요소 중 5개가 RaTG13에 존재하지 않기 때문이다"고 팀은 보고했다.
이것은 위치 403의 양전하를 띤 아미노산이 평균 이상으로 중요함을 시사한다. 이것은 역 교환에 의해 확인됐다. Zech와 그의 동료들이 발견한 바와 같이 아르기닌 대신 트레오닌이 포함된 SARS-CoV-2 슈도바이러스는 감염성이 감소했다. 대유행 병원체는 그렇지 않으면 우리 세포에 최적으로 적응되지만, 이 하나의 돌연변이는 결합 능력을 감소시키기에 충분했다.
추가 종 점프에 대한 요구 사항?
연구팀은 코로나바이러스의 종 도약을 위한 결정적인 단계를 찾을 수 있었다.
Zech와 그의 동료들은 "종합적으로 볼 때, 우리의 결과는 스파이크 단백질의 위치 403에 있는 양성 아미노산 단위가 효율적인 인수공통전염병 전염과 SARS-CoV-2의 대유행 확산을 위한 전제 조건임을 시사한다"고 기술했다.
동시에 이 결과는 동물계와 특히 박쥐에 이미 이 중요한 특성을 가진 많은 코로나바이러스가 있을 수 있음을 시사한다. 라오스 박쥐 바이러스와 천산갑 바이러스도 자연적으로 403번 위치에 양전하를 띤 아미노산을 가지고 있다.
최소한의 위안: 보충 테스트에서 백신 접종 및 회복기 환자의 인간 혈청 항체도 RaTG13의 인위적으로 돌연변이된 균주에 대해 작용했다. 많은 유전적 차이에도 불구하고 현재의 코로나 백신은 밀접하게 관련된 코로나바이러스와 미래의 인수공통전염병으로부터 보호할 수도 있다.
"따라서 Covid-19 백신 접종은 그러한 바이러스 병원체가 미래에 인간에게 퍼지는 것을 방지하는 데 도움이 될 수 있다"고 Zech와 그의 동료들이 설명했다.
(Nature Communications, 2021; doi: 10.1038 / s41467-021-27180-0)
출처: Universität Ulm
[더사이언스플러스 The SCIENCE Plus]
[저작권자ⓒ the SCIENCE plus. 무단전재-재배포 금지]
주요기사
+
많이 본 기사
Basic Science
+
AI & Tech
+
Photos
+