5분 읽기
- 배양균으로 실험 하던 미생물학자 알렉산더 플레밍은 실수로 배양균을 남겨두고 휴가 떠나
- 록펠러 재단 지원으로 1944년에 대규모 산업 생산이 시작되면서 항생제 시대가 열렸다.
- 1950년대 후반-1960년대 초반, 전 세계 수천 명의 어린이가 짧은 사지를 가지고 태어나
- 치명적인 오류는 콘테르간의 활성 성분인 탈리도마이드가 두 가지 형태로 존재하기 때문에 발생
이 우연한 발견은 1929년 당시 큰 화제가 되었다. 제1차 세계대전은 막 끝나고 수많은 사람이 목숨을 잃은 참사였다. 많은 군인이 상처 감염으로 죽었는데, 이를 치료할 효과적인 방법은 없었다. 전쟁이 끝난 후에도 디프테리아, 결핵, 발진티푸스와 같은 질병이 주민들 사이에 퍼졌다. 박테리아 배양액의 깨끗한 영역은 곰팡이가 박테리아 병원균을 죽일 수 있다는 것을 보여주었다. 즉, 항생제 효과가 있었다.
페니실린의 엄청난 잠재력은 처음에는 거의 활용되지 않았다. 플레밍이 곰팡이를 명확하게 식별하고 분리하는 데는 시간이 걸리기 때문이었다. 다음 단계에서 연구진은 페니실린이 백혈구를 공격하지 않으므로 감염성 질환을 치료하는 데 적합하다는 것을 발견했다. 그 미생물학자는 자신의 연구 결과를 런던의 한 저널에 발표했지만, 그의 기사에 주목하는 사람은 거의 없었다. 따라서 페니실린은 처음에는 상처를 소독하는 데 표면적으로만 사용되었다.
곰팡이 낀 멜론을 성공적인 컨셉으로
다음 단계는 1941년까지 진행되지 않았다. 당시에는 독일이 영국을 침공할 가능성을 더 배제할 수 없었기 때문에 페니실린 연구는 미국으로 이전되었고 록펠러 재단의 자금 지원을 받았다. 플레밍의 페트리 접시 속 무작위 방문객보다 더 빠르게 성장하는 균주를 찾는 표적 검색이 시작되는 곳이 바로 여기였다. 미국 공군은 전 세계에서 토양 샘플을 수집하고 있었다.
그리고 다시 한번 우연이 역할을 했다. 가장 생산적인 품종이 연구소 바로 앞 곰팡이 낀 멜론에서 발견되고 분리되었다. 1944년에 대규모 산업 생산이 시작되면서 항생제 시대가 열렸다.
노르웨이 버섯, 장기 이식에 도움
페니실린의 우연한 발견에 관한 이야기는 자연스럽게 널리 알려지게 되었다. 여전히 새로운 항생제가 필요하기 때문에, 우연에 약간의 도움을 주고자 하는 회사들이 곧 생겼을 것이다. 노르웨이에서 채취한 간단한 토양 샘플이 20세기의 가장 위대한 의학적 업적 중 하나인 장기 이식에 혁명을 일으켰다.
노르웨이 토양 샘플에서 과학자들은 다시 한번 살균 성질을 가진 곰팡이 균을 찾고 있었다. 하지만 그들은 이와 관련하여 아무것도 발견하지 못했다. 그러나 토양에서 추출한 다른 물질의 약리학적 효과를 조사하기 위한 추가 분석이 계획되어 있었다. 그중 하나가 신체의 면역 체계에 영향을 미치는 것으로 밝혀졌다.
장기 이식에 대한 도박은 더 없다.
1970년에 발견된 사이클로스포린의 특징은 이 물질이 림프구 배양을 선택적으로 억제한다는 것이다. 따라서 면역 체계의 일부만 억제되고, 감염 위험이 낮아지며 장기가 이물질로 인식되지 않는다. 의학계에서는 이 새로운 활성 성분의 잠재력을 금세 알아봤고, 1982년에는 전 세계적으로 시클로스포린이 이식 수술에 성공적으로 사용되기 시작했다. 간, 심장, 췌장 이식 후 환자의 생존율이 극적으로 향상되었다.
비극적인 결과를 초래한 반성
1950년대 후반과 1960년대 초반, 전 세계 수천 명의 어린이가 장기 기형과 짧은 사지를 가지고 태어났다. 부모들은 절망했고, 의사들은 어찌할 바를 몰랐다. 1961년 11월, 수면제 '콘테르간'이 기형의 원인이라는 의심이 제기되었다. 세포 배양과 동물 실험을 포함한 모든 예비 시험을 통과했으며 부작용이 전혀 나타나지 않은 약물이었다. 무엇이 잘못되었나?
왼손잡이 형태로 인한 기형
치명적인 오류는 콘테르간의 활성 성분인 탈리도마이드가 두 가지 형태로 존재하기 때문에 발생했을 수 있다. 우측 성분과 좌측 성분은 있다. 탈리도마이드는 키랄 물질이다. 두 분자는 같은 구조를 가지고 있지만 거울상처럼 행동한다.
이러한 "핸디드니스"를 지닌 분자에서는 종종 두 개의 거울상 이성질체 중 하나만이 생물학적으로 활성을 갖는다. 다른 변종은 가장 좋은 경우에는 유기체에 전혀 영향을 미치지 않지만, 최악의 경우에는 부정적인 영향을 미친다. 후자는 탈리도마이드에도 적용된다. 우선회전형은 거의 부작용 없이 잘 견디는 수면 보조제 역할을 하지만, 좌선회전형은 기형을 유발하며 임신 중에 복용하면 알려진 기형을 일으킨다.
당시, Contergan의 개발자들은 무해한 형태의 약물만 테스트했지만, 약물 합성 과정에서 라세미체가 형성되었는데, 이는 두 광학이성체가 50:50 비율로 혼합된 것이다. 그 당시에는 키랄 분자에 대한 지식이 오늘날만큼 발달하지 않았지만, 아무도 예측할 수 없었던 비극적인 우연의 일치를 믿고 싶어하지 않는 사람이 여전히 많았다.
나병과 암에 대한 지금의 도움
수면제를 생산한 그뤼넨탈 회사의 경영진은 여전히 너무 적은 양의 실험을 수행했다는 비난을 받고 있었다. 콘테르간 제조업체에 대한 재판은 1970년에 중단되었고 그뤼넨탈 회사는 자발적으로 피해자들에게 1억 1,400만 마르크를 지불했다. 그 이후로, 특히 임신 중에 약물을 복용하는 것이 위험하다는 인식이 크게 높아졌다.
무해한 우선회전형 탈리도마이드는 더 수면제로 사용되지 않는다. 흥미롭게도, 기형을 일으키는 왼손 형태가 계속해서 생산되고 있다. 세포 분열에 세포독소 역할을 하기 때문에 의학계에서는 현재 왼손잡이 거울상 이성질체를 나병 치료제로 사용하고 있으며, 특히 미국과 브라질에서 많이 사용한다. 독일에서는 탈리도마이드가 혈액암 치료제로 승인되었다. (계속)
- 배양균으로 실험 하던 미생물학자 알렉산더 플레밍은 실수로 배양균을 남겨두고 휴가 떠나
- 록펠러 재단 지원으로 1944년에 대규모 산업 생산이 시작되면서 항생제 시대가 열렸다.
- 1950년대 후반-1960년대 초반, 전 세계 수천 명의 어린이가 짧은 사지를 가지고 태어나
- 치명적인 오류는 콘테르간의 활성 성분인 탈리도마이드가 두 가지 형태로 존재하기 때문에 발생
의학에서의 행복한 우연과 불행한 우연
버려진 실험실에 몇 개의 페트리 접시가 홀로 잊혀 있었다. 포도상구균 배양액은 냉장고에서 자라므로 냉장고에 보관해야 했다. 하지만 배양균으로 실험을 하던 미생물학자 알렉산더 플레밍은 실수로 배양균을 남겨두고 휴가를 떠났다. 일부 곰팡이 포자가 눈에 띄지 않게 껍질 속으로 침투하여 그곳에서 자라기 시작했다.
망가진 시도
플레밍이 휴가에서 돌아왔을 때, 그는 큰 충격을 받았다. 그의 배양물 중 일부는 죽었고, 실험은 끝났다. 그 대신, 녹색 곰팡이의 일종인 균류가 페트리 접시 속으로 퍼졌다. Penicillinum notatum이라는 곰팡이다. 하지만 플레밍은 그 배양물을 바로 폐기하지 않고 좀 더 자세히 살펴보았다. 그는 곰팡이 군집 주변에 박테리아가 자라지 않는 깨끗한 구역을 보았다.
 |
| ▲ 1943년 런던의 연구실에 있는 알렉산더 플레밍. © gemeinfrei |
이 우연한 발견은 1929년 당시 큰 화제가 되었다. 제1차 세계대전은 막 끝나고 수많은 사람이 목숨을 잃은 참사였다. 많은 군인이 상처 감염으로 죽었는데, 이를 치료할 효과적인 방법은 없었다. 전쟁이 끝난 후에도 디프테리아, 결핵, 발진티푸스와 같은 질병이 주민들 사이에 퍼졌다. 박테리아 배양액의 깨끗한 영역은 곰팡이가 박테리아 병원균을 죽일 수 있다는 것을 보여주었다. 즉, 항생제 효과가 있었다.
페니실린의 엄청난 잠재력은 처음에는 거의 활용되지 않았다. 플레밍이 곰팡이를 명확하게 식별하고 분리하는 데는 시간이 걸리기 때문이었다. 다음 단계에서 연구진은 페니실린이 백혈구를 공격하지 않으므로 감염성 질환을 치료하는 데 적합하다는 것을 발견했다. 그 미생물학자는 자신의 연구 결과를 런던의 한 저널에 발표했지만, 그의 기사에 주목하는 사람은 거의 없었다. 따라서 페니실린은 처음에는 상처를 소독하는 데 표면적으로만 사용되었다.
곰팡이 낀 멜론을 성공적인 컨셉으로
다음 단계는 1941년까지 진행되지 않았다. 당시에는 독일이 영국을 침공할 가능성을 더 배제할 수 없었기 때문에 페니실린 연구는 미국으로 이전되었고 록펠러 재단의 자금 지원을 받았다. 플레밍의 페트리 접시 속 무작위 방문객보다 더 빠르게 성장하는 균주를 찾는 표적 검색이 시작되는 곳이 바로 여기였다. 미국 공군은 전 세계에서 토양 샘플을 수집하고 있었다.
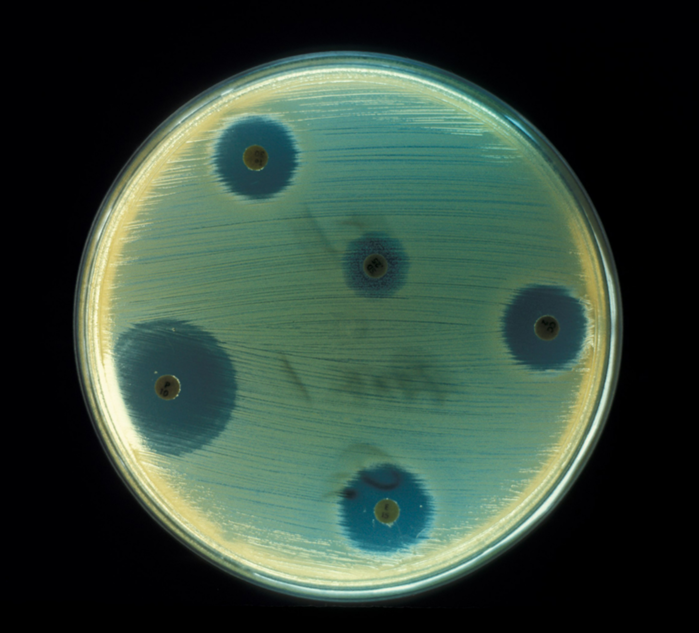 |
| ▲ 황색포도상구균(Staphylococcus aureus)은 항생제 정제 주변에서 성장이 나타나지 않았다. © CDC/Don Stalons |
그리고 다시 한번 우연이 역할을 했다. 가장 생산적인 품종이 연구소 바로 앞 곰팡이 낀 멜론에서 발견되고 분리되었다. 1944년에 대규모 산업 생산이 시작되면서 항생제 시대가 열렸다.
노르웨이 버섯, 장기 이식에 도움
페니실린의 우연한 발견에 관한 이야기는 자연스럽게 널리 알려지게 되었다. 여전히 새로운 항생제가 필요하기 때문에, 우연에 약간의 도움을 주고자 하는 회사들이 곧 생겼을 것이다. 노르웨이에서 채취한 간단한 토양 샘플이 20세기의 가장 위대한 의학적 업적 중 하나인 장기 이식에 혁명을 일으켰다.
노르웨이 토양 샘플에서 과학자들은 다시 한번 살균 성질을 가진 곰팡이 균을 찾고 있었다. 하지만 그들은 이와 관련하여 아무것도 발견하지 못했다. 그러나 토양에서 추출한 다른 물질의 약리학적 효과를 조사하기 위한 추가 분석이 계획되어 있었다. 그중 하나가 신체의 면역 체계에 영향을 미치는 것으로 밝혀졌다.
장기 이식에 대한 도박은 더 없다.
1970년에 발견된 사이클로스포린의 특징은 이 물질이 림프구 배양을 선택적으로 억제한다는 것이다. 따라서 면역 체계의 일부만 억제되고, 감염 위험이 낮아지며 장기가 이물질로 인식되지 않는다. 의학계에서는 이 새로운 활성 성분의 잠재력을 금세 알아봤고, 1982년에는 전 세계적으로 시클로스포린이 이식 수술에 성공적으로 사용되기 시작했다. 간, 심장, 췌장 이식 후 환자의 생존율이 극적으로 향상되었다.
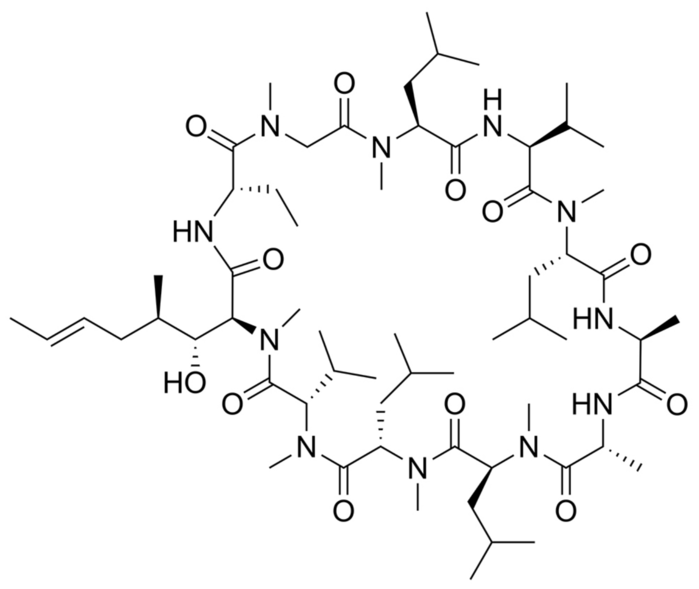 |
| ▲ 시클로스포린은 균류인 Tolypocladium inflatum과 Clindrocarpon lucidum에서 유래한 면역억제제다. © Yikrazuul/ gemeinfrei |
비극적인 결과를 초래한 반성
1950년대 후반과 1960년대 초반, 전 세계 수천 명의 어린이가 장기 기형과 짧은 사지를 가지고 태어났다. 부모들은 절망했고, 의사들은 어찌할 바를 몰랐다. 1961년 11월, 수면제 '콘테르간'이 기형의 원인이라는 의심이 제기되었다. 세포 배양과 동물 실험을 포함한 모든 예비 시험을 통과했으며 부작용이 전혀 나타나지 않은 약물이었다. 무엇이 잘못되었나?
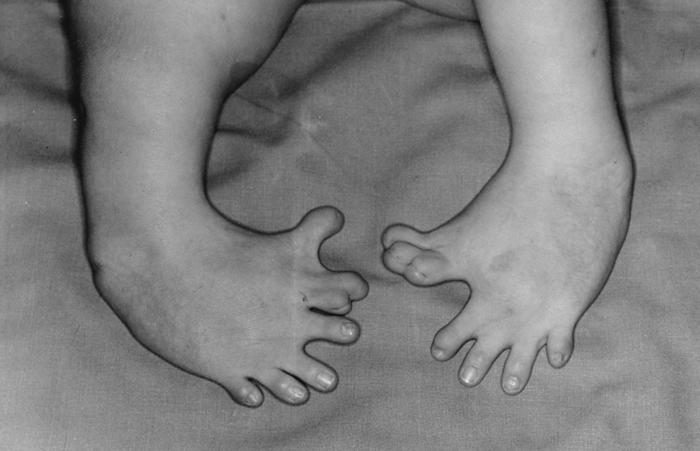 |
| ▲ 임신 중에 탈리도마이드를 복용한 어머니의 많은 아이들은 자궁에서 다리와 팔의 기형을 보였다. © otisarchives3/ CC-by 2.0 |
왼손잡이 형태로 인한 기형
치명적인 오류는 콘테르간의 활성 성분인 탈리도마이드가 두 가지 형태로 존재하기 때문에 발생했을 수 있다. 우측 성분과 좌측 성분은 있다. 탈리도마이드는 키랄 물질이다. 두 분자는 같은 구조를 가지고 있지만 거울상처럼 행동한다.
이러한 "핸디드니스"를 지닌 분자에서는 종종 두 개의 거울상 이성질체 중 하나만이 생물학적으로 활성을 갖는다. 다른 변종은 가장 좋은 경우에는 유기체에 전혀 영향을 미치지 않지만, 최악의 경우에는 부정적인 영향을 미친다. 후자는 탈리도마이드에도 적용된다. 우선회전형은 거의 부작용 없이 잘 견디는 수면 보조제 역할을 하지만, 좌선회전형은 기형을 유발하며 임신 중에 복용하면 알려진 기형을 일으킨다.
당시, Contergan의 개발자들은 무해한 형태의 약물만 테스트했지만, 약물 합성 과정에서 라세미체가 형성되었는데, 이는 두 광학이성체가 50:50 비율로 혼합된 것이다. 그 당시에는 키랄 분자에 대한 지식이 오늘날만큼 발달하지 않았지만, 아무도 예측할 수 없었던 비극적인 우연의 일치를 믿고 싶어하지 않는 사람이 여전히 많았다.
나병과 암에 대한 지금의 도움
수면제를 생산한 그뤼넨탈 회사의 경영진은 여전히 너무 적은 양의 실험을 수행했다는 비난을 받고 있었다. 콘테르간 제조업체에 대한 재판은 1970년에 중단되었고 그뤼넨탈 회사는 자발적으로 피해자들에게 1억 1,400만 마르크를 지불했다. 그 이후로, 특히 임신 중에 약물을 복용하는 것이 위험하다는 인식이 크게 높아졌다.
무해한 우선회전형 탈리도마이드는 더 수면제로 사용되지 않는다. 흥미롭게도, 기형을 일으키는 왼손 형태가 계속해서 생산되고 있다. 세포 분열에 세포독소 역할을 하기 때문에 의학계에서는 현재 왼손잡이 거울상 이성질체를 나병 치료제로 사용하고 있으며, 특히 미국과 브라질에서 많이 사용한다. 독일에서는 탈리도마이드가 혈액암 치료제로 승인되었다. (계속)
[더사이언스플러스=문광주 기자]
[저작권자ⓒ the SCIENCE plus. 무단전재-재배포 금지]
주요기사
+
많이 본 기사
Basic Science
+
AI & Tech
+
Photos
+